政策法規(guī)||本周重磅政策法規(guī)概覽(21.09.26-21.09.30)
01
關(guān)于公開征求《化學(xué)仿制藥晶型研究技術(shù)指導(dǎo)原則(征求意見稿)》意見的通知
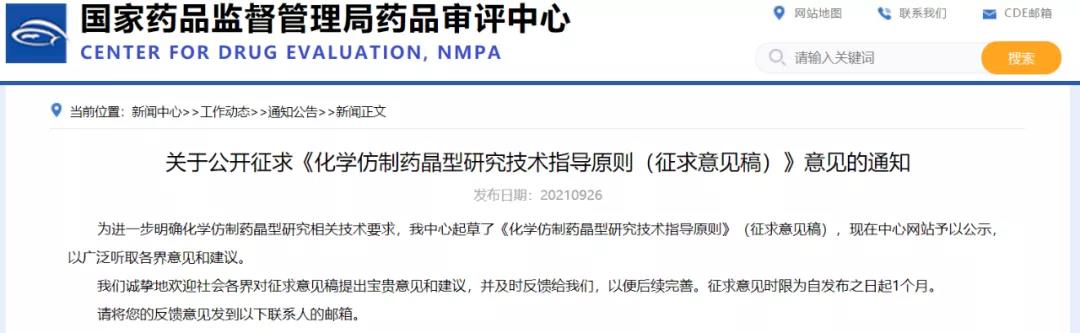
掃描下方二維碼
查看詳細(xì)信息

關(guān)于公開征求《口服固體制劑混合均勻度和中控劑量單位均勻度研究技術(shù)指導(dǎo)原則(征求意見稿)》意見的通知

掃描下方二維碼
查看詳細(xì)信息

關(guān)于公開征求《對(duì)我國<以藥動(dòng)學(xué)參數(shù)為終點(diǎn)評(píng)價(jià)指標(biāo)的化學(xué)藥物仿制藥人體生物等效性研究技術(shù)指導(dǎo)原則>中關(guān)于多規(guī)格豁免BE藥學(xué)評(píng)價(jià)標(biāo)準(zhǔn)“處方比例相似性”相關(guān)問題的問答(征求意見稿二)》意見的通知

掃描下方二維碼
查看詳細(xì)信息

01
1.本周共發(fā)布了271個(gè)品規(guī)的藥品批準(zhǔn)證明文件待領(lǐng)取信息,其中一致性評(píng)價(jià)25個(gè),注射劑33個(gè)。

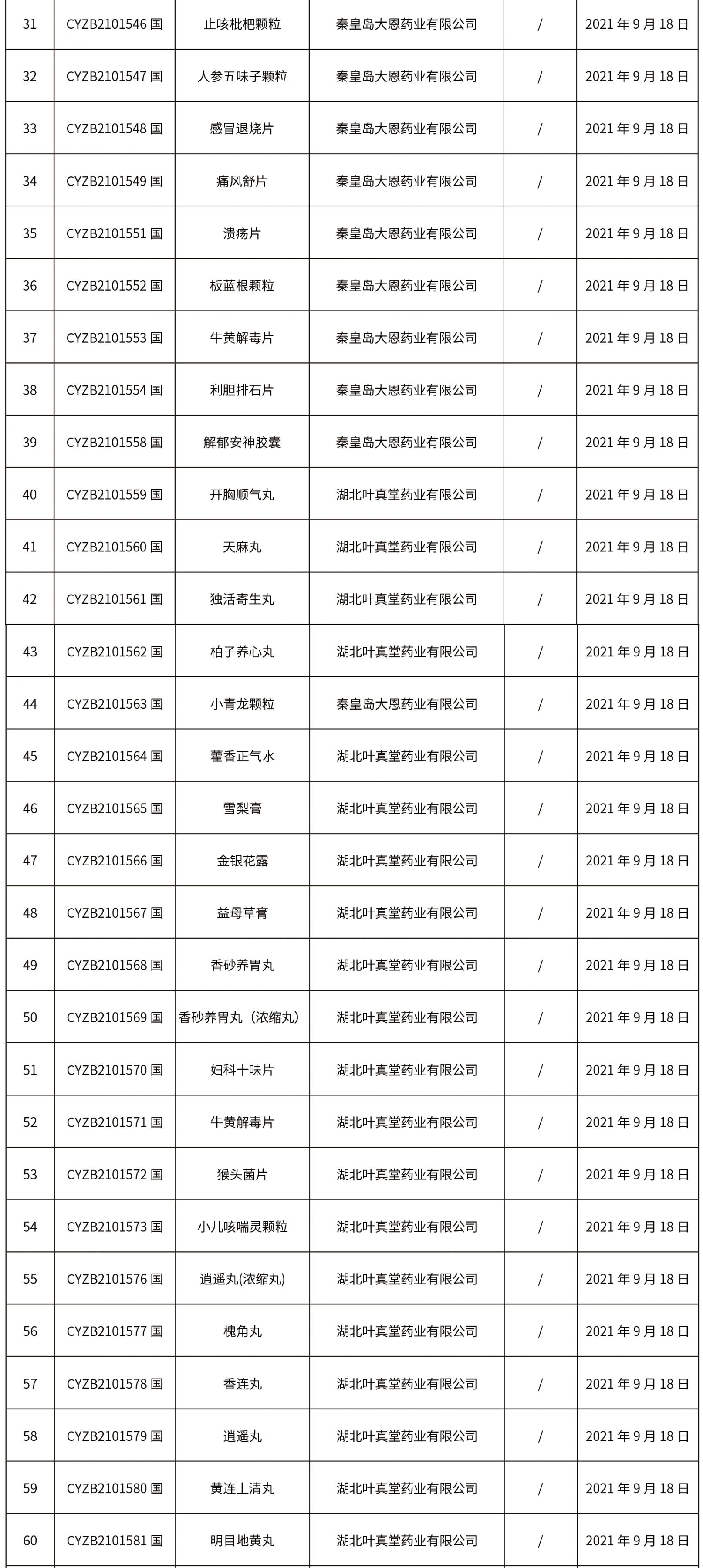
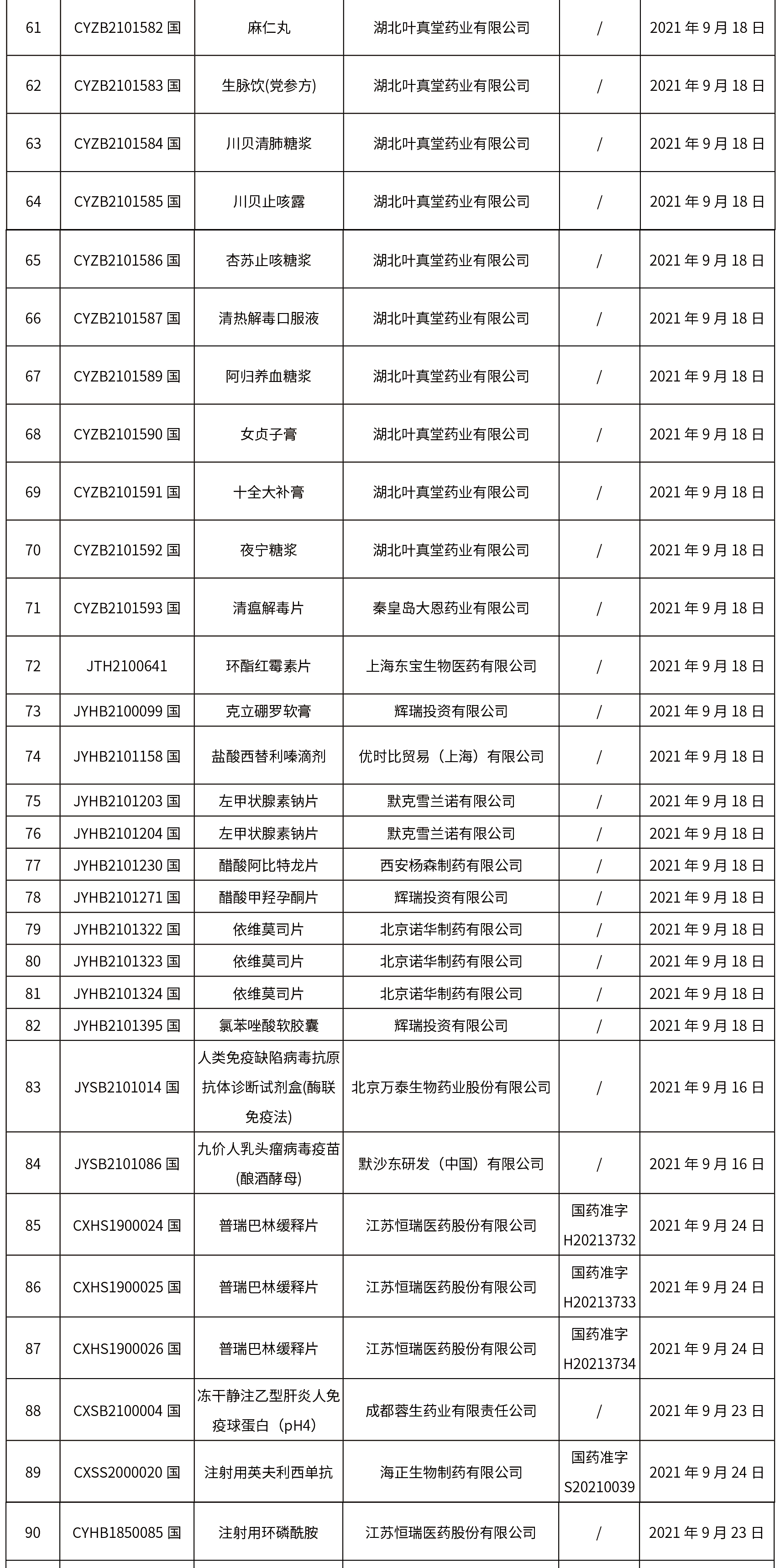
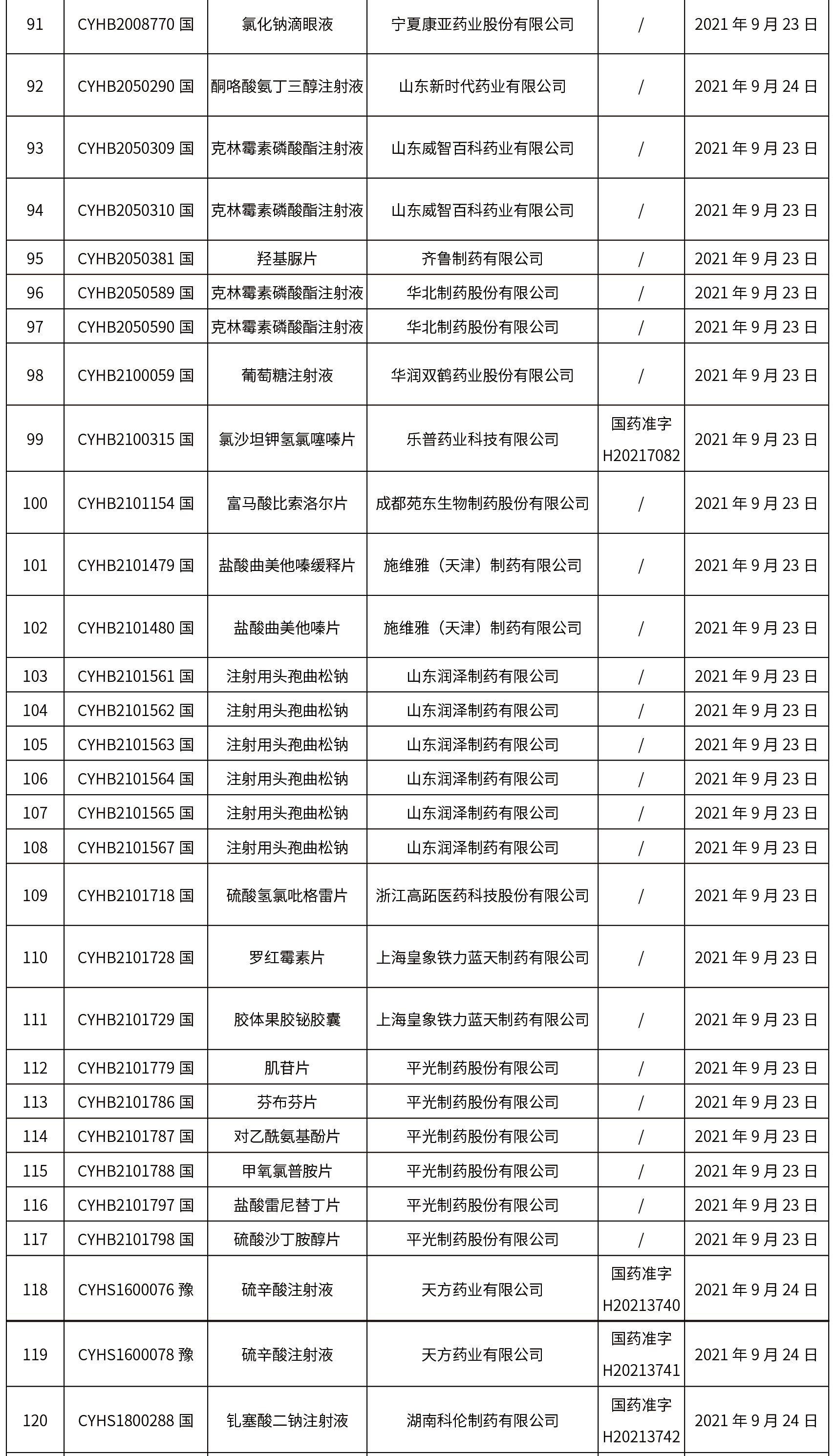
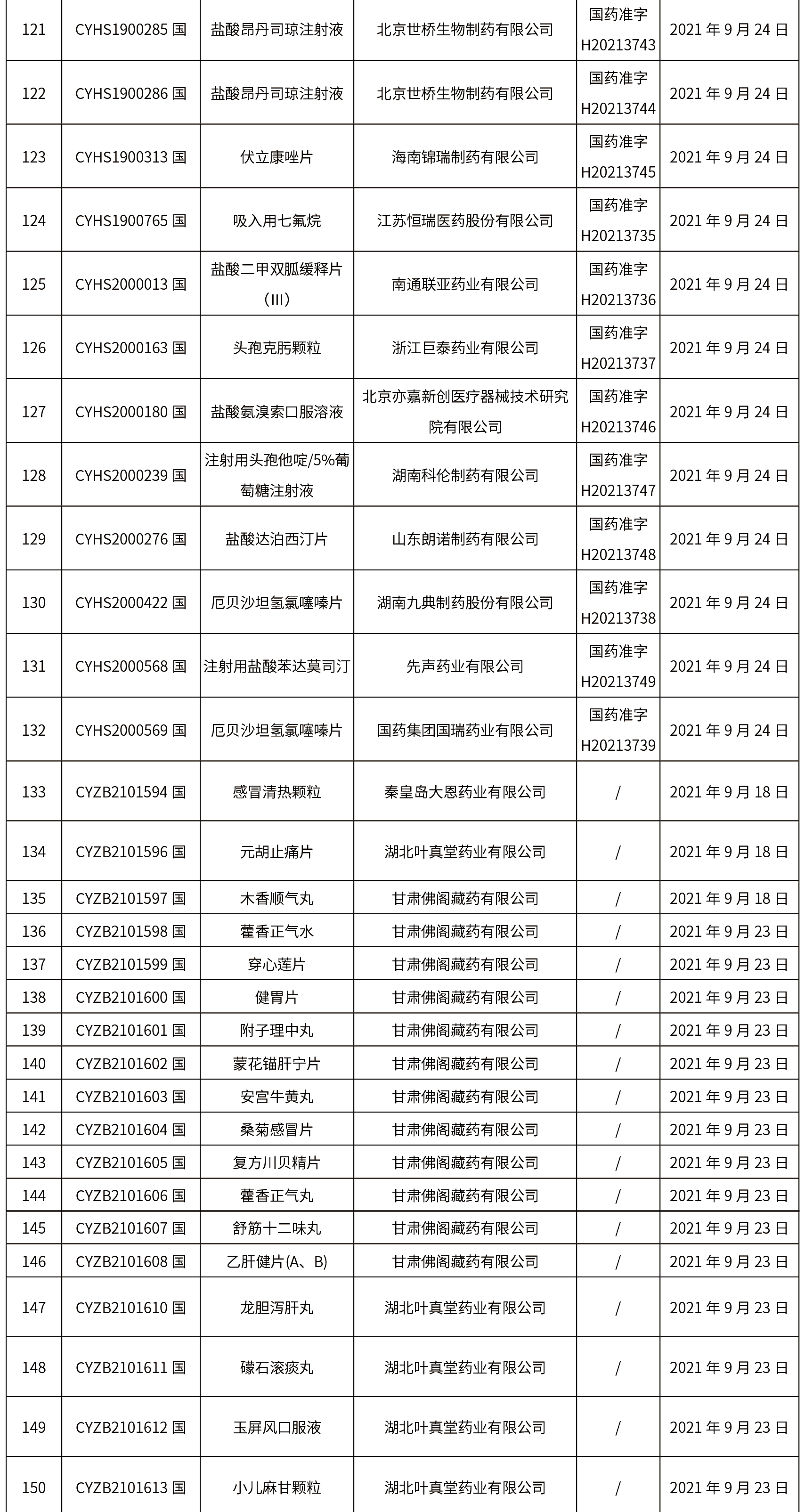
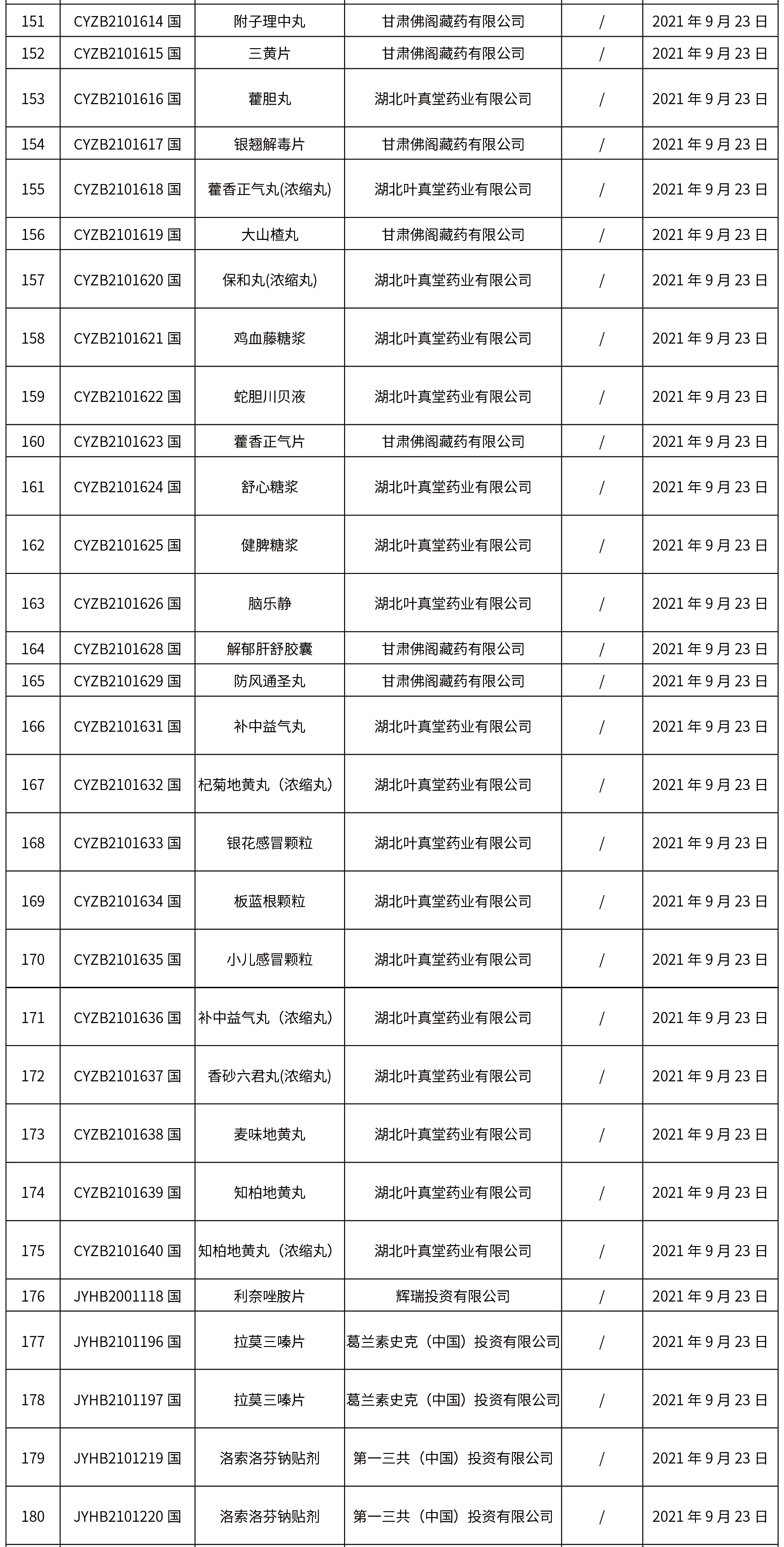

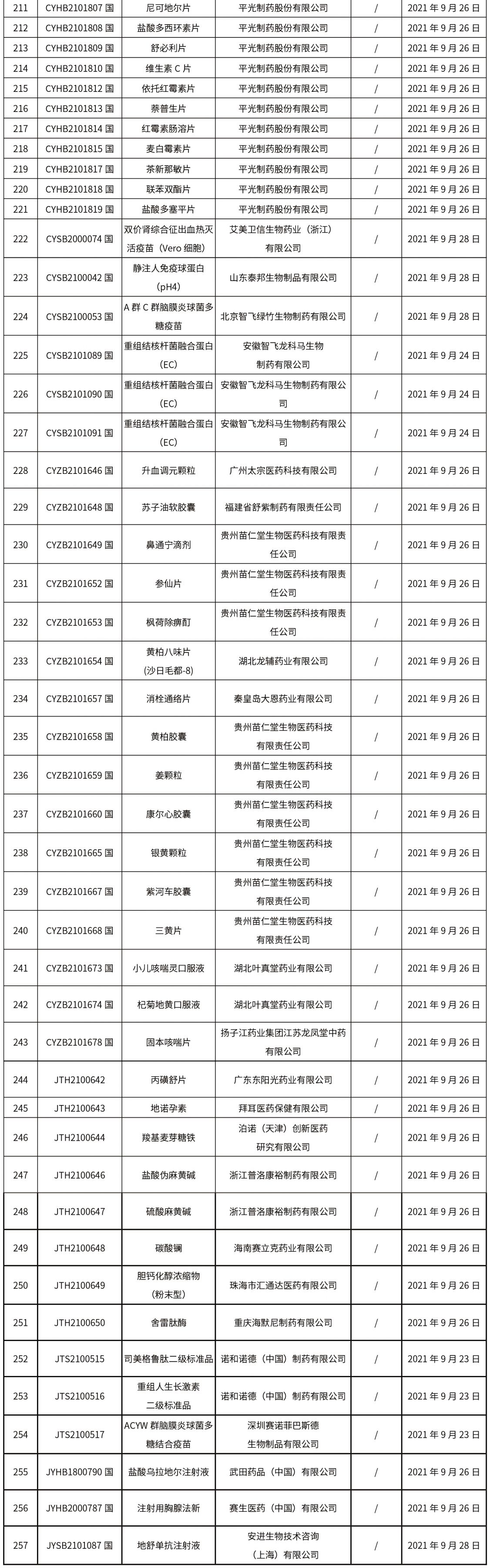
02
關(guān)于公布體外診斷試劑注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告(2021年第122號(hào))
掃描下方二維碼
查看詳細(xì)信息

03
關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告(2021年第121號(hào))

掃描下方二維碼
查看詳細(xì)信息

04
國家藥監(jiān)局關(guān)于實(shí)施藥品電子通用技術(shù)文檔申報(bào)的公告(2021年第119號(hào))
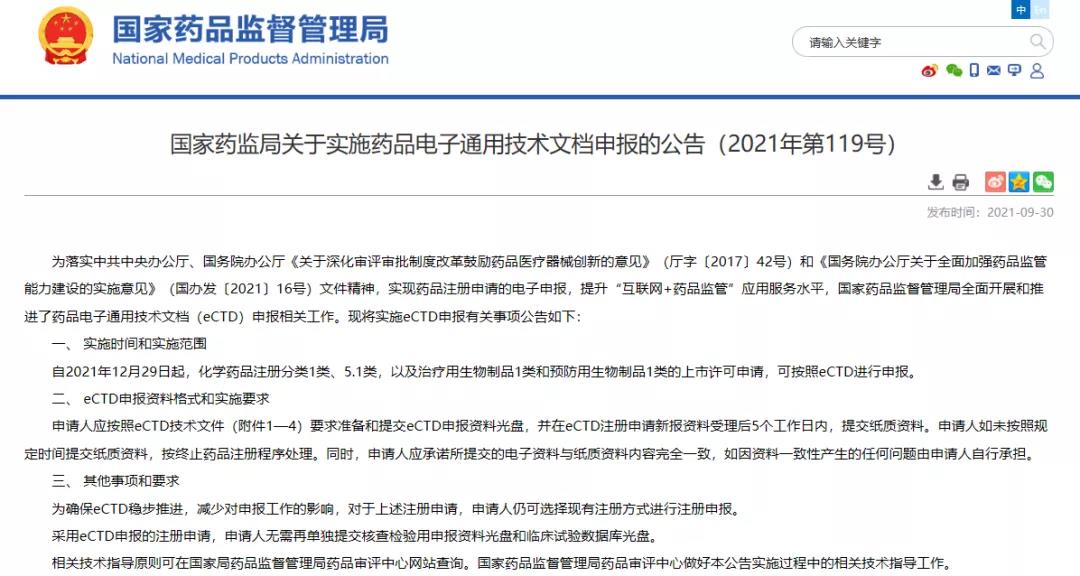
掃描下方二維碼
查看詳細(xì)信息

05
國家藥品監(jiān)督管理局關(guān)于順鉑注射劑等品種說明書增加兒童用藥信息的公告(2021年第118號(hào))

掃描下方二維碼
查看詳細(xì)信息

06
國家藥品監(jiān)督管理局關(guān)于實(shí)施《醫(yī)療器械注冊(cè)與備案管理辦法》《體外診斷試劑注冊(cè)與備案管理辦法》有關(guān)事項(xiàng)的通告(2021年第76號(hào))

掃描下方二維碼
查看詳細(xì)信息

07
國家藥監(jiān)局關(guān)于發(fā)布醫(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則等5項(xiàng)技術(shù)指導(dǎo)原則的通告(2021年第73號(hào))

掃描下方二維碼
查看詳細(xì)信息

08
國家藥監(jiān)局關(guān)于成立全國醫(yī)療器械臨床評(píng)價(jià)標(biāo)準(zhǔn)化技術(shù)歸口單位的公告(2021年第116號(hào))

掃描下方二維碼
查看詳細(xì)信息

09
國家藥監(jiān)局關(guān)于蘆薈珍珠膠囊處方藥轉(zhuǎn)換為非處方藥的公告(2021年第115號(hào))

掃描下方二維碼
查看詳細(xì)信息

10
國家藥監(jiān)局關(guān)于發(fā)布醫(yī)療器械動(dòng)物試驗(yàn)研究注冊(cè)審查指導(dǎo)原則 第一部分:決策原則(2021年修訂版)等2項(xiàng)注冊(cè)審查指導(dǎo)原則的通告(2021年第75號(hào))

掃描下方二維碼
查看詳細(xì)信息

11
國家藥監(jiān)局關(guān)于發(fā)布體外診斷試劑臨床試驗(yàn)技術(shù)指導(dǎo)原則的通告(2021年第72號(hào))

掃描下方二維碼
查看詳細(xì)信息

01
藥品注冊(cè)申請(qǐng)藥學(xué)研制和生產(chǎn)現(xiàn)場核查任務(wù)信息公告(2021年第22號(hào))

掃描下方二維碼
查看詳細(xì)信息

02
藥品注冊(cè)申請(qǐng)藥學(xué)研制和生產(chǎn)現(xiàn)場檢查任務(wù)信息公告(2021年第21號(hào))
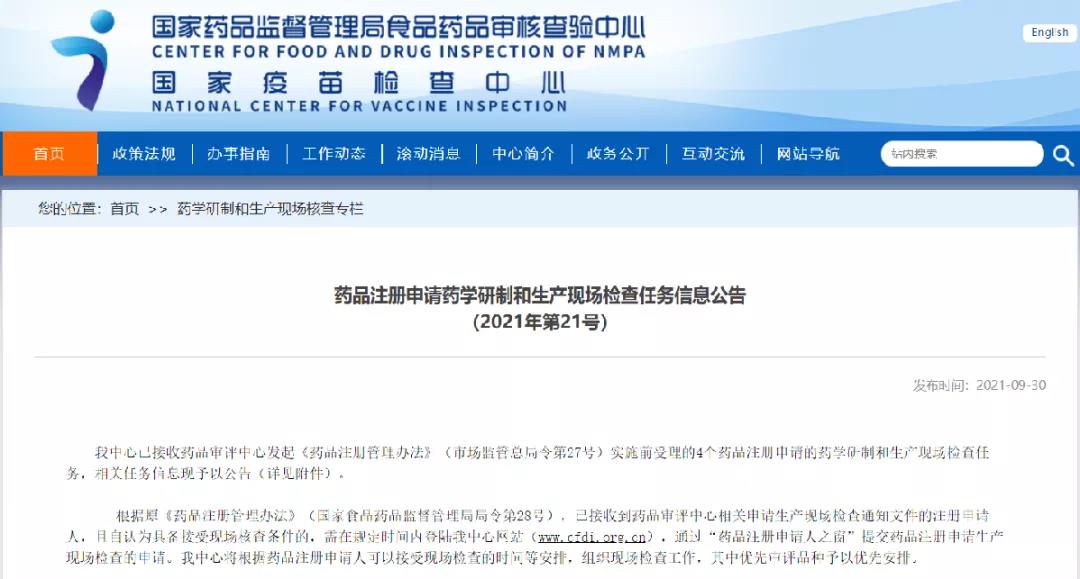
掃描下方二維碼
查看詳細(xì)信息

1.本周發(fā)布4個(gè)品種的國家藥品標(biāo)準(zhǔn)公示。

掃描下方二維碼
查看詳細(xì)信息

轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來源:新領(lǐng)先醫(yī)藥科技”。

 Hotline服務(wù)熱線:010-61006450
Hotline服務(wù)熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場部:
技術(shù)市場部: 北京新領(lǐng)先
北京新領(lǐng)先 新領(lǐng)先藥訊
新領(lǐng)先藥訊 010-61006450
010-61006450
