市場 | 淺析吸入制劑概況及市場前景
吸入制劑主要用于慢性呼吸系統(tǒng)疾病的治療,慢性呼吸系統(tǒng)疾病高居我國居民死亡原因的第三位,僅次于心腦血管疾病和腫瘤。
哮喘和慢性阻塞性肺病(COPD)是最為常見的慢病呼吸系統(tǒng)疾病,近年來隨著呼吸系統(tǒng)疾病患病率上升以及人們對哮喘、COPD 等疾病的深入了解,首選吸入給藥途徑治療上述疾病已成為全球共識。
經(jīng)口吸入制劑 ( orally inhaled drug products,OIDPS) 指通過吸入途徑將藥物遞送至呼吸道和/或肺部以發(fā)揮局部或全身作用的制劑。
-
與普通口服制劑相比,吸入制劑的藥物可直接到達吸收或作用部位,吸收或作用快,可避免肝臟首過效應、減少用藥劑量;
-
與注射制劑相比,吸入制劑可提高患者依從性,同時可減輕或避免部分藥物不良反應。
與傳統(tǒng)劑型不同,大多數(shù)經(jīng)口吸入制劑被設計為局部作用于肺部,主要有霧化吸入劑(nebulizer,也稱噴霧劑)、壓力定量吸入劑(pMDI,也稱氣霧劑) 和干粉吸入劑(DPI,也稱吸入粉霧劑) ,針對其作用機制及優(yōu)缺點見下表。

常見的慢病呼吸系統(tǒng)疾病所用吸入制劑類型藥物包括短效β2 受體激動劑(SABA)、長效β2 受體激動劑(LABA) 、短效膽堿能拮抗劑(SAMA) 、長效膽堿能拮抗劑(LAMA) 及吸入性糖皮質(zhì)激素(ICS) 等,常見藥物如下表。
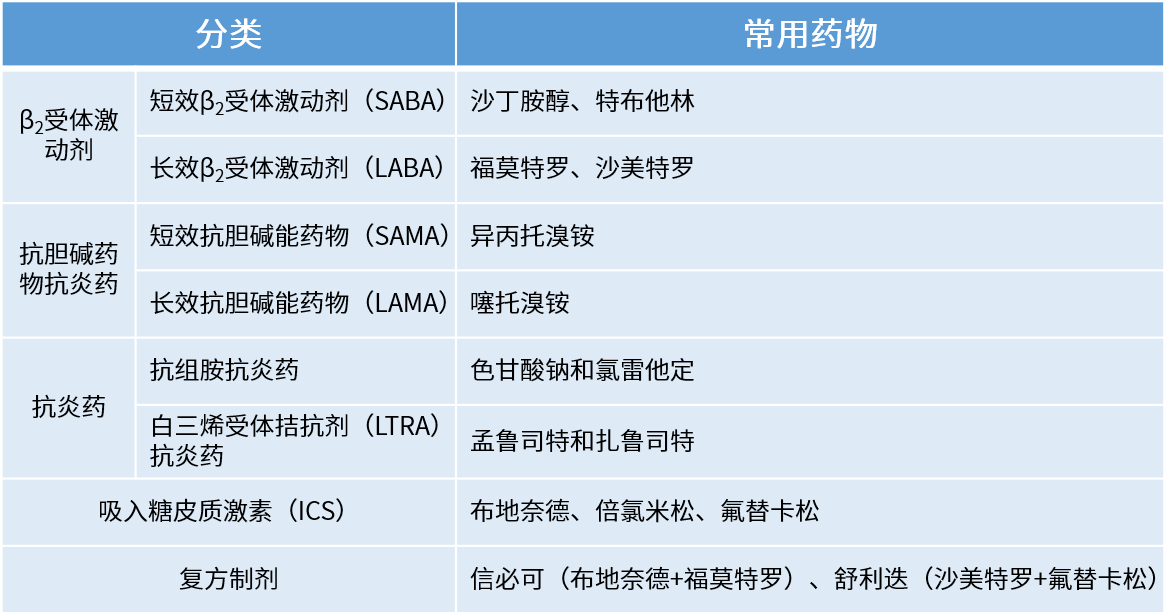
治療哮喘的藥物主要分為兩類:
-
控制類藥物,即需要每天使用并長時間維持應用的藥物,包括吸入性糖皮質(zhì)激素(ICS)、ICS/長效β2受體激動劑(ICS/LABA)、全身性激素、白三烯調(diào)節(jié)劑(LTRA)、緩釋茶堿、抗IgE單克隆抗體等;
-
緩解類藥物,急性發(fā)作時使用,主要通過迅速解除支氣管痙攣來緩解哮喘癥狀,以支氣管舒張類藥物為主,包括速效和短效口服β2受體激動劑(SABA)、ICS/福莫特羅、全身性激素、吸入型抗膽堿能藥物、短效茶堿等。
COPD治療以支氣管擴張劑為核心。支氣管擴張劑通過改變氣道平滑肌的張力引起氣道擴張,規(guī)律使用可有效預防或減輕COPD癥狀, 主要包括β2受體激動劑和抗膽堿能拮抗劑。
根據(jù)GOLD推薦,COPD起始治療通常以長效β2受體激動劑(LABA)和/或長效抗膽堿能拮抗劑(LAMA)為主,對于中度至極重度COPD患者,ICS聯(lián)合LABA改善肺功能和健康狀況及減少急性加重較單藥有效。
〖1〗仿制難度較高:
-
吸入制劑需藥品和吸入裝置聯(lián)合使用,以MDI為例,其一般由主藥物、輔料(拋射劑)、耐壓容器、定量閥門系統(tǒng)和噴射裝置組成,主要質(zhì)量控制指標包括藥物的粒度及粒度分布、噴射模式、每噴主藥含量以及每瓶總噴次等。
-
藥物的吸入裝置專利時間通常比藥物專利保護期長,仿制難度進一步提升。
〖2〗吸入制劑的生物等效性評價存在其特殊性:
吸入制劑的生物等效性評價是體外藥學與體內(nèi)臨床研究相結(jié)合的一個過程。體外研究需要充分考察吸入制劑粒徑、裝置等指標,體內(nèi)研究需要判斷常規(guī)的PK方法是否能夠充分評估生物等效性。
受試試劑與參比制劑在體外藥學質(zhì)量一致的情況下,一般采用藥動學、藥效學或臨床終點等方法進行生物等效性研究。
〖3〗BE標準的建立正逐步完善:
大多數(shù)吸入產(chǎn)品是復雜的劑型,其整合了配方和裝置,增加了其BE建立的復雜性。
因此,目前全球只有部分國家或組織頒布了局部作用的經(jīng)口吸入制劑BE 指導原則,如美國食品藥品管理局(FDA) 、歐洲藥品局(EMA) 、澳大利亞藥品管理局(TGA) 等。針對具體藥物,F(xiàn)DA 于2010 年開始,陸續(xù)公布《特定藥物的生物等效性指導原則》,并持續(xù)更新藥物品種和內(nèi)容。
科學規(guī)范和指導藥物研究工作,原國家食品藥品監(jiān)督管理局(CFDA) 于2007年組織制定了《吸入制劑質(zhì)量控制研究技術(shù)指導原則》。國家藥品監(jiān)督管理局(NMPA) 于2021 年公布《經(jīng)口吸入制劑仿制藥藥學和人體生物等效性研究指導原則》,進一步推進和指導仿制藥質(zhì)量和療效一致性評價工作。
從全球呼吸系統(tǒng)主要吸入制劑的生產(chǎn)廠家來看,用藥市場基本被GSK、AZ和BI三家藥企壟斷。目前國家出臺一系列政策,鼓勵大力發(fā)展高端仿制藥,打破壁壘,進口替代大幕已經(jīng)緩緩拉開。
全球呼吸系統(tǒng)主要吸入制劑

- 自2016年化藥新注冊分類起至2018年底,NMPA首次批準上市的吸入制劑僅6個,而且全部是按老Ⅵ類注冊申報的,其中4個還是用于化痰的吸入用乙酰半胱氨酸溶液,市場規(guī)模較小,獲批后還需進行一致性評價。另外兩個是麻醉用藥。
- 2019年4月9日,健康元吸入用復方異丙托溴銨溶液以新Ⅳ類注冊申請獲批,是國內(nèi)第一個通過一致性評價的呼吸系統(tǒng)吸入制劑。健康元復方異丙托溴銨與經(jīng)典代表性品種阿斯利康的普米克令舒(布地奈德混懸液)一樣,都是通過霧化裝置幫助吸入,仿制難度與MDI相比同樣不小。本次獲批意味著國內(nèi)部分企業(yè)已經(jīng)具備了仿制高端吸入制劑品種的能力,進口企業(yè)的壟斷地位將被打破。
目前布地奈德混懸液、布地奈德福莫特羅粉吸入劑、沙美特羅替卡松粉吸入劑等重磅品種國內(nèi)僅原研獲批,市場被原研企業(yè)獨占。國內(nèi)企業(yè)正在重磅品種積極布局,一旦首仿成功,有望快速實現(xiàn)進口替代。
本土藥企及CRO在采用藥動學參數(shù)進行生物等效性研究評價仿制藥積累了大量經(jīng)驗,但是吸入制劑進行藥效學或臨床終點等方法進行生物等效性研究還鮮有開展,經(jīng)驗較少,挑戰(zhàn)巨大,可預見未來如何成功組織實施PD-BE將是藥企及CRO的新的戰(zhàn)略高地。
-END-



轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應在授權(quán)范圍內(nèi)使用,并注明“來源:新領(lǐng)先醫(yī)藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場部:
技術(shù)市場部: 北京新領(lǐng)先
北京新領(lǐng)先 新領(lǐng)先藥訊
新領(lǐng)先藥訊 010-61006450
010-61006450
