CRC 須知!試驗用藥品管理
試驗用藥是一種在臨床試驗中供試驗的或作為對照的活性成分或安慰劑的藥物制劑。為了確保受試者權(quán)益,保證臨床試驗質(zhì)量,臨床試驗用藥品的接收、保存、發(fā)放、回收、清點、銷毀,都必須符合試驗方案和相關(guān)法規(guī)要求。
-
標準:遵循GCP的原則以及試驗藥物管理的sop。
-
執(zhí)行:
(1)委派符合資格的人員。
(2)相關(guān)人員進行試驗藥物管理培訓。
(3)所有藥品相關(guān)的試驗資料應(yīng)當被準確記錄,妥善保存。
-
檢查/核實:
(1)試驗藥物的制備應(yīng)當符合臨床試驗用藥品生產(chǎn)質(zhì)量管理相關(guān)要求。
(2)試驗藥物的使用應(yīng)當符合試驗方案。
? 申辦方/CRO
負責研究藥物的生產(chǎn)、供應(yīng)、包裝、運輸,具體包括:
-
保證藥品質(zhì)量合格(GMP生產(chǎn)、易于識別、正確編碼)。
-
建立試驗藥物管理和記錄系統(tǒng)。
-
負責向研究中心提供試驗藥物(安全送達藥物、保存相關(guān)文件、回收試驗藥物、處置未使用試驗藥物)。
? 研究者
熟悉了解試驗藥物,負責試驗藥物的使用;掌握臨床試驗進行期間發(fā)現(xiàn)的所有與藥物有關(guān)的信息。研究者必須保障:
-
所有研究藥物僅用于臨床試驗的受試者。
-
劑量與用法需要遵照試驗方案。
-
剩余的試驗用藥退回申辦方。
-
由專人管理研究藥物。
? CRC或其他指定人員
(一)負責藥物管理的實際工作,需要具備藥物管理資格:
-
具備相應(yīng)的專業(yè)背景(藥學/護理學等)。
-
獲得研究者的授權(quán)。
-
接受研究藥物管理的培訓。
(二)負責藥物管理的專項工作:
-
藥物管理的過程均須記錄。
-
接受相關(guān)人員對藥物管理工作的檢查。
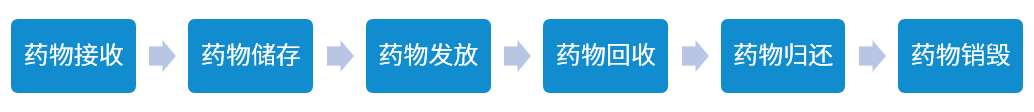
? 試驗用藥物的接收
(一)在試驗開始前
CRC應(yīng)確認試驗用藥品存放的地點、環(huán)境、接收地址、接收人及聯(lián)系方式。
(二)試驗用藥品到達后
-
CRC (或協(xié)助藥物管理員)接收,并與藥物運單核對,包括藥物名稱、數(shù)量、藥物批號、藥物編號、規(guī)格、劑型、有效期等。
-
CRC (或協(xié)助藥物管理員)填寫藥物接收的表格及藥物庫存表。
-
CRC (或協(xié)助藥物管理員)負責保管運送藥物的溫度計,確保儀器完好可用。
-
CRC (或協(xié)助藥物管理員)核對完所有藥物信息并確認無誤后,立即通過IVRS/IWRS等途徑確認接收藥物,收到確認文件后再次與藥物信息核對,無誤后打印簽字,并保存。
? 試驗用藥物的儲存
-
CRC (或協(xié)助藥物管理員)對試驗用藥品保存的環(huán)境應(yīng)定期進行核查:干燥、通風、整潔、衛(wèi)生、無污染及污染源,并做好防火、防塵、防潮、防蟲及防鼠等相應(yīng)管理工作。
-
CRC應(yīng)確認試驗用藥品按項目存放,專人專柜加鎖保管,并根據(jù)方案要求進行藥物儲存。
-
CRC (或協(xié)助藥物管理員)依照方案要求記錄溫度、濕度,若發(fā)現(xiàn)溫、濕度異常,應(yīng)及時與監(jiān)查員溝通,并協(xié)助藥物管理員尋找原因并解決,記錄儲存條件偏離的時間、所儲存的藥品數(shù)量、藥物編號等,報方案偏離。
-
CRC (或協(xié)助藥物管理員)應(yīng)定期檢查藥物有效期,發(fā)現(xiàn)過期藥物應(yīng)及時與藥物管理員及監(jiān)查員聯(lián)系;針對過期藥物,按照申辦方的要求處理。
-
CRC應(yīng)確認有效藥物與過期藥物、回收藥物與未分發(fā)藥物均已分開放置,并有明顯標注。
-
CRC (或藥物管理員)應(yīng)確保一定數(shù)量的庫存。
-
需要特殊保存條件的藥物,應(yīng)根據(jù)相應(yīng)要求制定藥物保存的核查規(guī)定。
? 試驗用藥物的發(fā)放
-
分發(fā)藥物應(yīng)由被授權(quán)的藥物管理員或CRC進行,這些人員在試驗開始前應(yīng)接受并完成藥物管理的相關(guān)培訓。
-
通過隨機系統(tǒng)獲取研究藥品編號時,CRC需首先輸入項目號、中心號、受試者編號、性別、出生日期、訪視日期、訪視周期、劑量調(diào)整等信息,然后確認輸入的信息是否準確,在獲取確認文件后再次確認。
-
CRC (或協(xié)助藥物管理員)應(yīng)根據(jù)藥品發(fā)放的確認文件,及醫(yī)囑或處方領(lǐng)取相應(yīng)編號的試驗用藥品,并及時在“藥品發(fā)放回收登記表”記錄。
-
分發(fā)試驗用藥品前,CRC (或藥物管理員)應(yīng)與研究者或指定研究人員雙方再次核對藥物編號、受試者編號、隨訪周期等信息是否與確認文件中的信息一致,確保藥品的準確發(fā)放。發(fā)給受試者時,由受試者確認后在簽收單上簽字,即發(fā)藥的每個步驟都需要確認。
-
CRC (或協(xié)助藥物管理員)提醒受試者剩余的試驗用藥品(包括無論何種原因未使用的藥物)需要回收,必須在下一次隨訪時將剩余藥物及用藥日記卡帶回研究中心。
? 試驗用藥物的回收
-
CRC(或協(xié)助藥物管理員)回收受試者每次的剩余藥物、藥盒或藥板,應(yīng)認真清點并記錄在“藥物發(fā)放回收記錄表”中。
-
CRC若發(fā)現(xiàn)剩余藥量與實際應(yīng)歸還的數(shù)量不一致,或者發(fā)現(xiàn)服藥日記卡記錄的數(shù)量或時間點未符合方案要求時,需向受試者進行確認,了解是否有多服或漏服試驗用藥品,并再次指導受試者正確服藥以及告知其正確服藥的重要性,同時提醒研究者將真實情況記錄在病歷中。
? 試驗用藥物的歸還
-
剩余的試驗藥物應(yīng)返回申辦方,封箱寄回(其他處置方法應(yīng)妥善記錄)。
-
必須記錄內(nèi)容包括:日期、數(shù)量、批號、有效期(如有)、分配的試驗用藥和受試者編碼。
? 試驗用藥物的銷毀
-
試驗過程中或結(jié)束后,CRC (或藥品管理員)應(yīng)確認需要銷毀的試驗用藥品,核對其數(shù)量與“藥品發(fā)放回收登記表”記錄的受試者歸還數(shù)量是否一致,同時做好銷毀記錄。
-
CRC (或藥物管理員)協(xié)助監(jiān)查員將需收回的試驗用藥品打包,監(jiān)查員填寫銷毀相關(guān)表格。藥物管理員與CRA雙人核對簽字,原件一式兩份,一份由中心存檔,一份由申辦方存檔。若為快遞運送,需存檔快遞單。
-
如在研究中心銷毀,CRC (或藥物管理員)保存申辦方的銷毀委托函,并對銷毀藥物的申辦方、項目號、藥物名稱、數(shù)量、銷毀時間、地點、參加人員等進行記錄,原件式兩份,一份由中心存檔, 一份由申辦方存檔。
-
非試驗相關(guān)人員不得接觸試驗用藥品。
-
試驗用藥品必須按照方案的要求妥善保存。
-
試驗用藥品的接收、分發(fā)、回收、清點、銷毀等必須有書面記錄。
-
試驗用藥品可由CRC直接管理及發(fā)放。
-
試驗用藥品儲存標簽應(yīng)擺放合理,以便觀察。
-END-


轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應(yīng)在授權(quán)范圍內(nèi)使用,并注明“來源:新領(lǐng)先醫(yī)藥科技”。

 Hotline服務(wù)熱線:010-61006450
Hotline服務(wù)熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場部:
技術(shù)市場部: 北京新領(lǐng)先
北京新領(lǐng)先 新領(lǐng)先藥訊
新領(lǐng)先藥訊 010-61006450
010-61006450
