政策法規||抗腫瘤光動力治療藥物臨床研發技術指導原則(征求意見稿)發布(附法規概覽11.21-11.25)
01
國家藥監局藥審中心關于發布《注射用兩性霉素B脂質體生物等效性研究技術指導原則》的通告(2022年第45號)
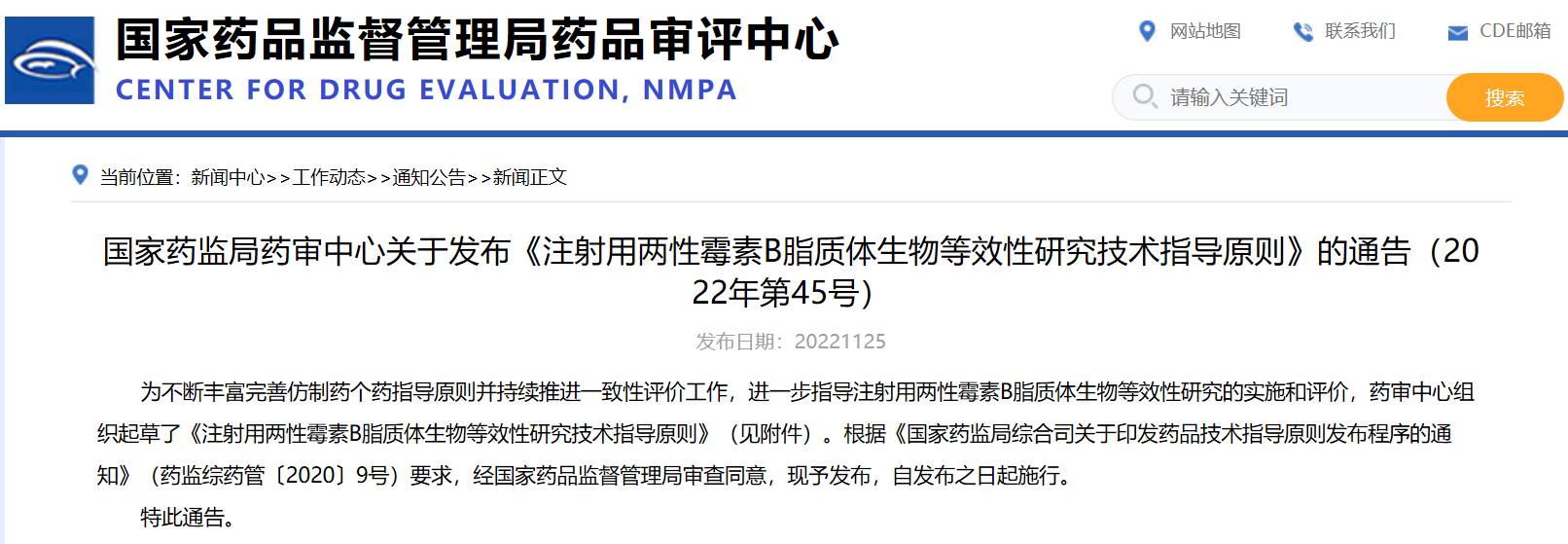
掃描識別圖中二維碼
查看詳細信息

02
國家藥監局藥審中心關于發布《他達拉非片生物等效性研究技術指導原則》的通告(2022年第44號)

掃描識別圖中二維碼
查看詳細信息

03

掃描識別圖中二維碼
查看詳細信息

04
國家藥監局藥審中心關于發布《富馬酸丙酚替諾福韋片生物等效性研究技術指導原則》的通告(2022年第42號)

掃描識別圖中二維碼
查看詳細信息

05
關于公開征求《抗腫瘤光動力治療藥物臨床研發技術指導原則(征求意見稿)》意見的通知

掃描識別圖中二維碼
查看詳細信息

06
國家藥監局藥審中心關于發布 《組織患者參與藥物研發的一般考慮指導原則(試行)》的通告(2022年第46號)

掃描識別圖中二維碼
查看詳細信息

本周法規
CDE
關于舉辦《ICH Q8(R2)—Q12指導原則線上培訓》的通知

掃描識別圖中二維碼
查看詳細信息

NMPA
1. 本周(截止到11.25下午12:40)共發布了40個品規的藥品批準證明文件待領取信息,其中一致性評價5個,注射劑29個。
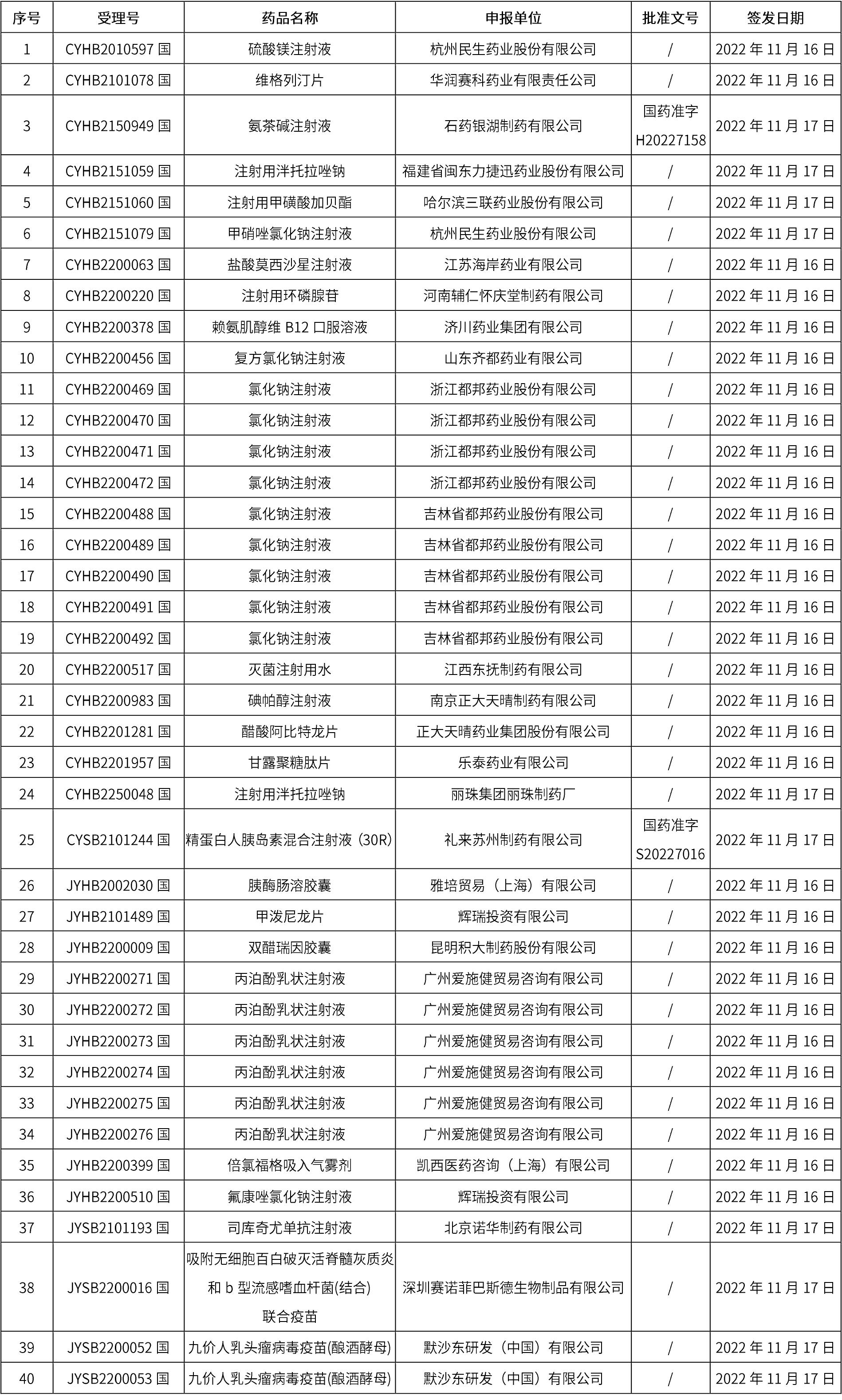
02
2022年11月23日中藥品種保護受理公示

掃描識別圖中二維碼
查看詳細信息

03
國家藥監局關于發布《化妝品中16α-羥基潑尼松龍的測定》化妝品補充檢驗方法的公告

掃描識別圖中二維碼
查看詳細信息

04
2022年11月24日中藥品種保護受理公示

掃描識別圖中二維碼
查看詳細信息

藥典委
本周藥典委發布人工牛黃、哮喘片國家藥品標準草案和藥包材生物學評價與試驗選擇指導原則草案的公示。
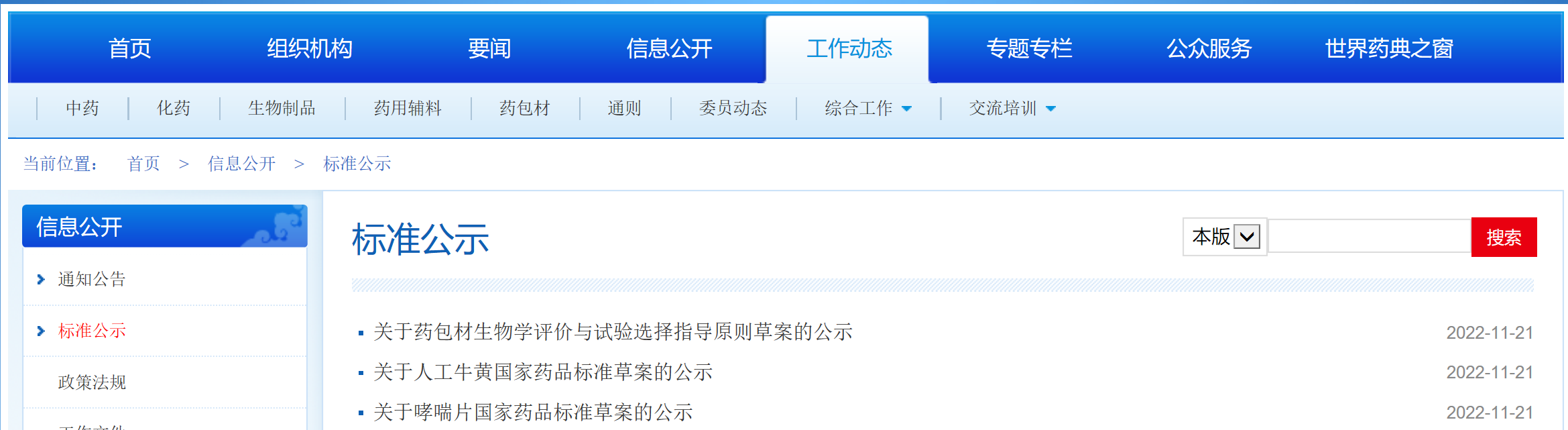
掃描識別圖中二維碼
查看詳細信息

-END-



轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
