政策法規 || 適用《Q9(R1):質量風險管理》國際人用藥品注冊技術協調會指導原則(附法規概覽09.04-09.08)
01
國家藥監局關于適用《Q9(R1):質量風險管理》國際人用藥品注冊技術協調會指導原則的公告(2023年第114號)
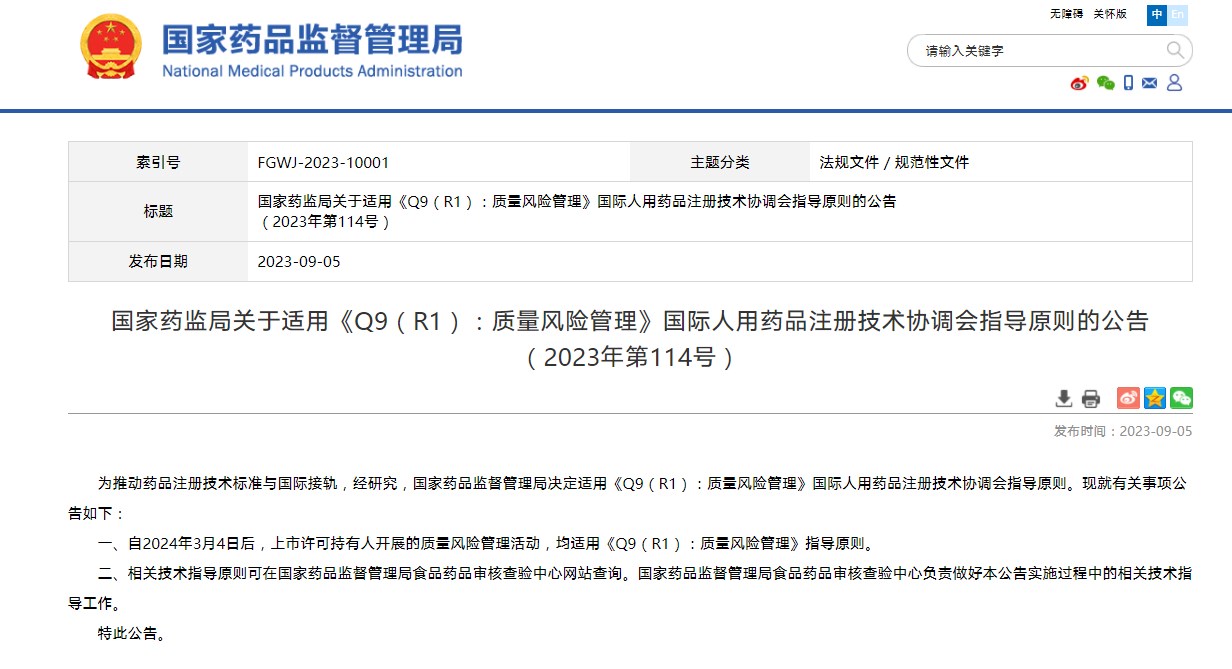
掃描識別圖中二維碼
查看詳細信息

02
國家藥監局綜合司公開征求《藥品網絡交易第三方平臺檢查指導原則》意見

掃描識別圖中二維碼
查看詳細信息

01
關于公開征求《人纖維蛋白原臨床試驗技術指導原則(修訂版征求意見稿)》意見的通知

掃描識別圖中二維碼
查看詳細信息

02
國家藥監局藥審中心發布《中國新藥注冊臨床試驗進展年度報告(2022年)》

掃描識別圖中二維碼
查看詳細信息

NMPA
01
截止2023年9月8日 16:00本周發布228個待領取藥品批準證明文件,其中注射液23個,一致性評價品種20個。
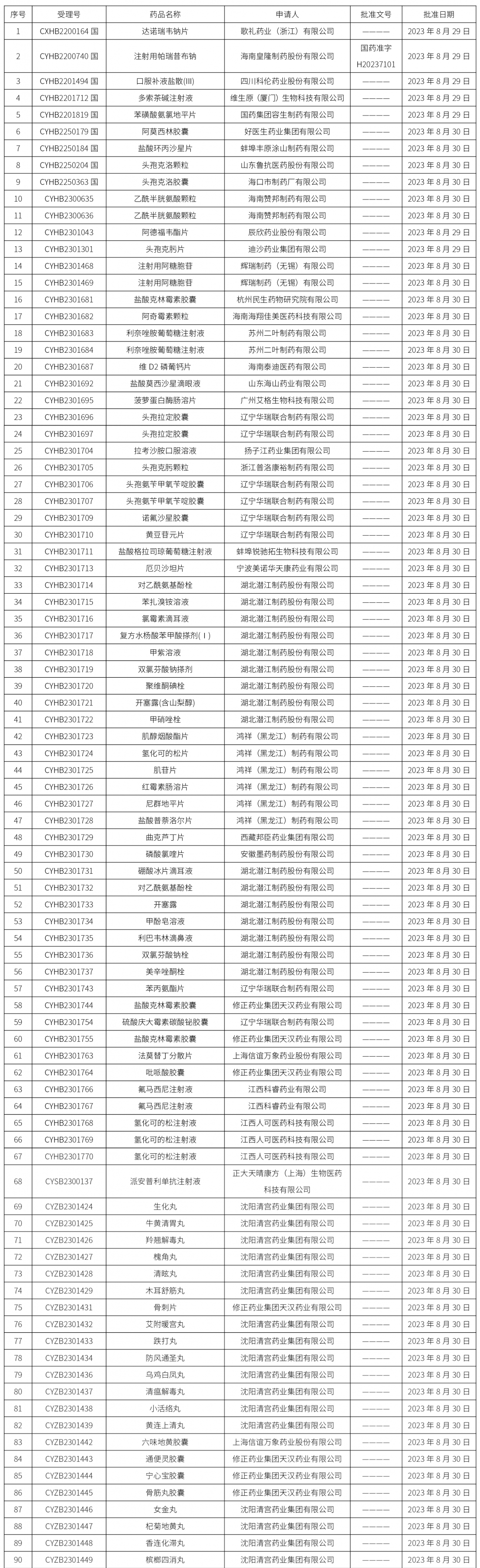
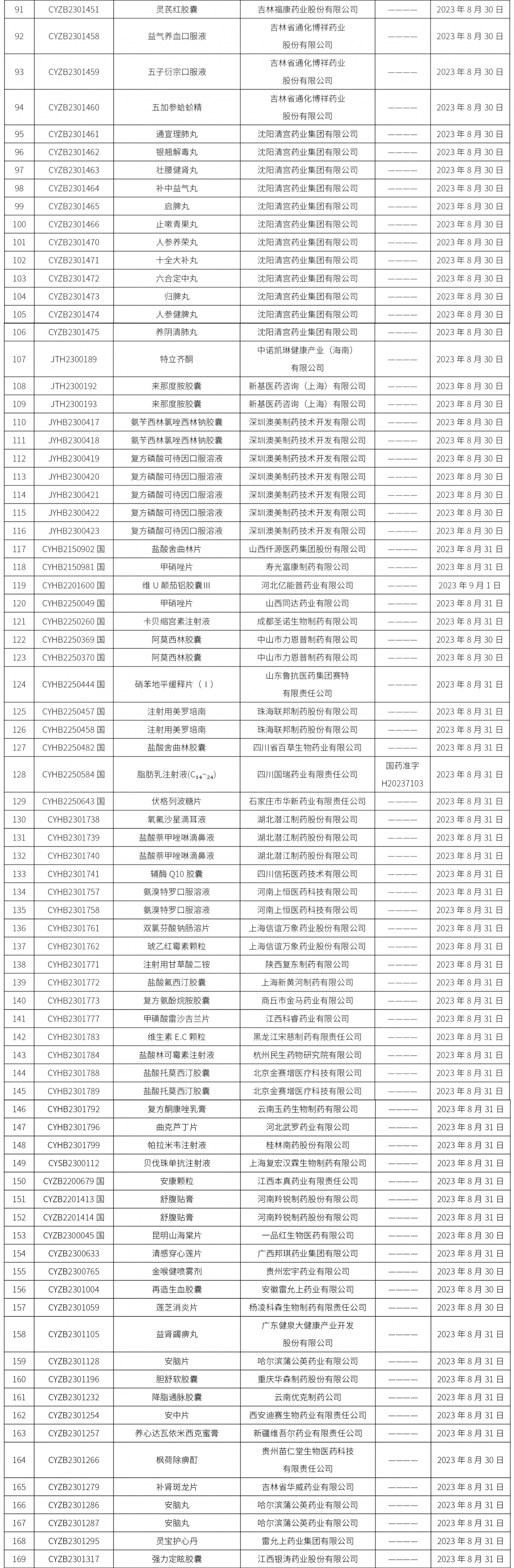
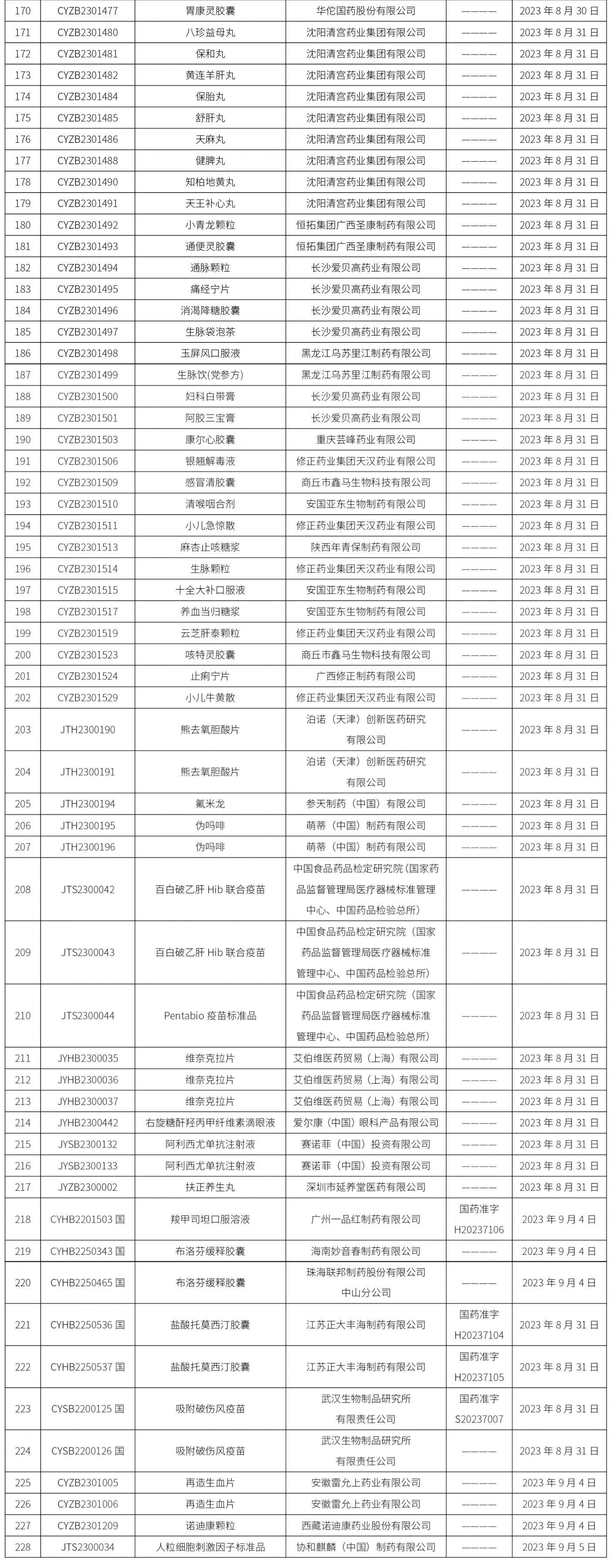
02
2023年9月4日中藥品種保護受理公示

掃描識別圖中二維碼
查看詳細信息

03
國家藥監局關于適用《S12:基因治療產品非臨床生物分布的考慮》國際人用藥品注冊技術協調會指導原則的公告(2023年第115號)
掃描識別圖中二維碼
查看詳細信息

04
國家藥監局綜合司關于提前終止有關中藥品種保護的通知
掃描識別圖中二維碼
查看詳細信息

05
國家藥監局關于注銷酶標儀醫療器械注冊證書的公告(2023年第116號)
掃描識別圖中二維碼
查看詳細信息

06
國家藥監局綜合司公開征求《藥品網絡交易第三方平臺檢查指導原則(征求意見稿)》意見

掃描識別圖中二維碼
查看詳細信息

07
國家藥監局關于發布YY 0304-2023《等離子噴涂羥基磷灰石涂層鈦基牙種植體》 等45項醫療器械行業標準的公告(2023年第118號)
掃描識別圖中二維碼
查看詳細信息

01
關于更新E2B(R3)實施指南問答文件中文稿的通知

掃描識別圖中二維碼
查看詳細信息

近期藥典委發布關于腦脈利顆粒、參芪五味子糖漿、參麥顆粒 國家藥品標準草案,關于磷酸氫鈣二水合物國家藥用輔料標準草案,關于制酸力測定法、0502 薄層色譜法、0901 溶液顏色檢查法、0902 澄清度檢查法、0521 氣相色譜法、0993 堆密度和振實密度測定法標準草案,關于化學成像、固有溶出測定指導原則標準草案的公示。
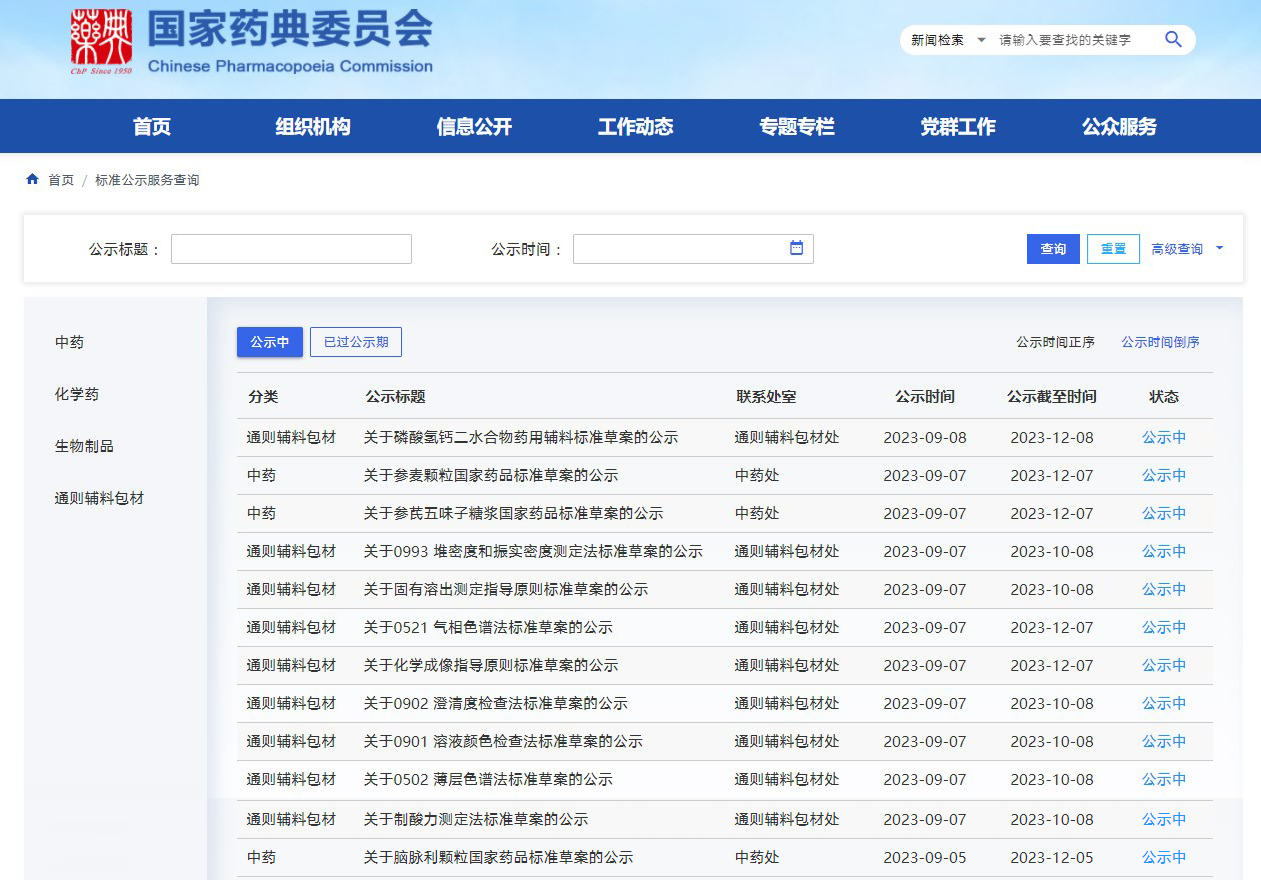
掃描識別圖中二維碼
查看詳細信息

-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
