文獻解讀 | 基于生理藥代動力學(PBPK)模型的食物效應預測案例研究
生理藥代動力學(PBPK)模型可以模擬化合物在空腹和餐后狀態下的藥代動力學參數。研究人員為了提高PBPK建模的實用性,利用生物藥劑學分類系統(BCS)I和II化合物的速釋制劑的現有臨床數據,對中等和高滲透性化合物吸收具有充分了解。
本文將通過案例研究展示如何使用建立、驗證模型,預測食物效應,整合初始模型開發的溶解度和溶出度數據,對餐后狀態下的臨床數據進行了驗證。
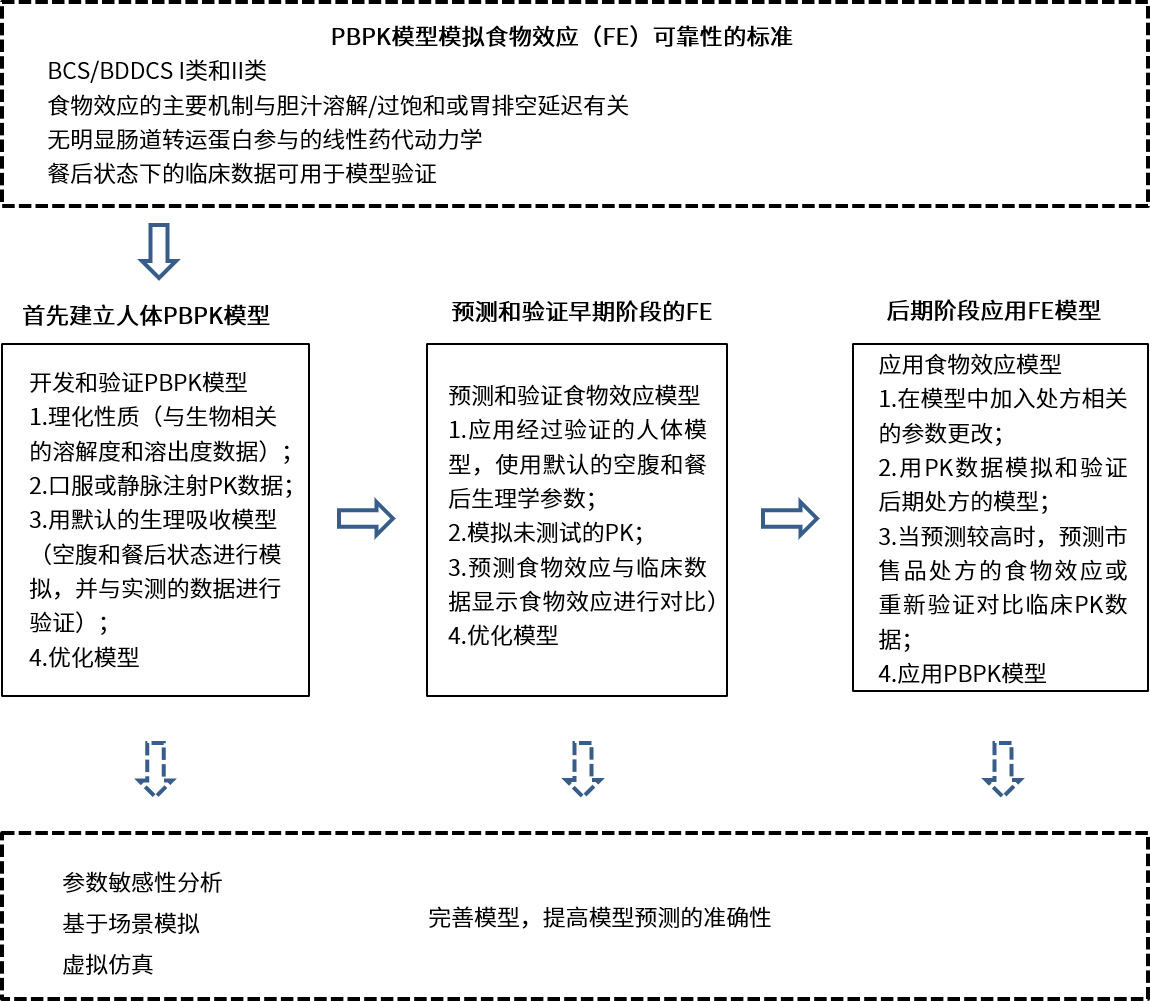
食物影響藥物吸收的因素
與空腹狀態給藥相比,口服藥物隨餐攝入可能會引起生物利用度的顯著變化,食物對生物利用度的影響會對藥物開發、監管和臨床環境產生重大影響。
-
食物對胃腸道的生理學和胃腸液的物理化學性質具有復雜而顯著的影響,這些影響的程度也取決于藥物的理化性質,主要包括溶解度、pKa、 LogP、logD,以及制劑特征(包括固體劑型的釋放和崩解)。
-
食物也可能影響胃腸道環境,改變其pH值,膽酸鹽濃度或粘度等,影響胃腸道生理條件,例如胃排空時間、腸道轉移時間、腸道轉移體或酶。
文獻研究案例分析
案例一:處方變更后BCS I類化合物食物效應的評估
化合物1作為一種簡單的活性藥物成分(API)在懸浮液/溶液中給藥,臨床研究中作為一種簡單的常規處方(膠囊)給藥。
-
化合物1在2.5至550mg的劑量范圍內對AUC和Cmax均表現出線性相關。
-
在80mg劑量下,高脂肪膳食(FDA標準早餐)對化合物1的AUC0-∞和Cmax均無影響,對于健康志愿者給予的80mg劑量,男性和女性受試者CL/生物利用度分別為24.2L/h和20.0L/h,男性和女性受試者中心分布容積分別為435L和326L。
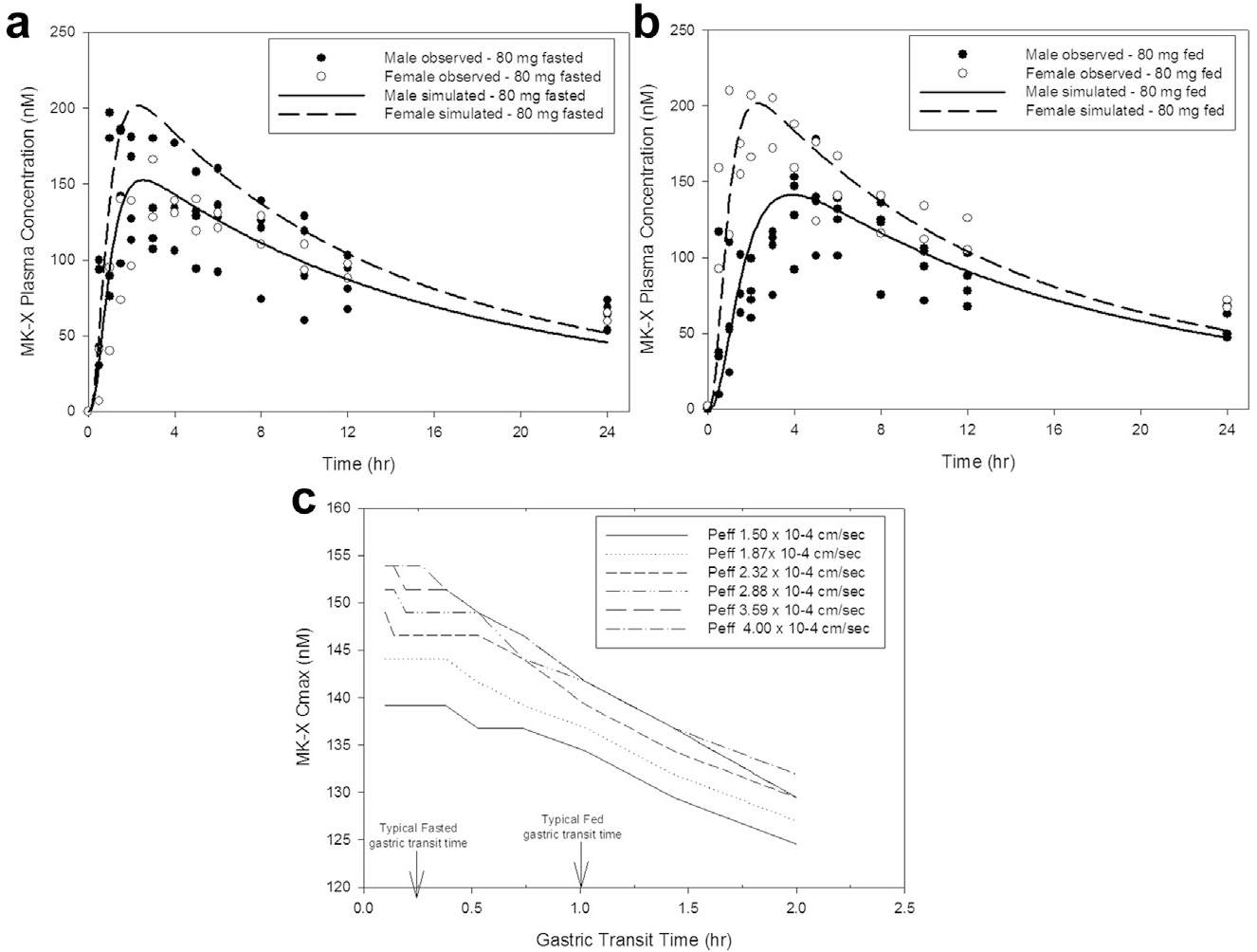
案例1分析:
(a)實測(點)與模型預測(線)的80mg劑量的化合物1的空腹藥時曲線
(b)實測(點)與模型預測(線)的80mg劑量的化合物1餐后狀態下的藥時曲線
(c)滲透性和胃排空時間對化合物1的Cmax在40mg劑量下影響的參數敏感性分析
參考這篇文獻案例1,小編運用GastroPlus軟件輸入文獻的相關參數,模擬結果如下:
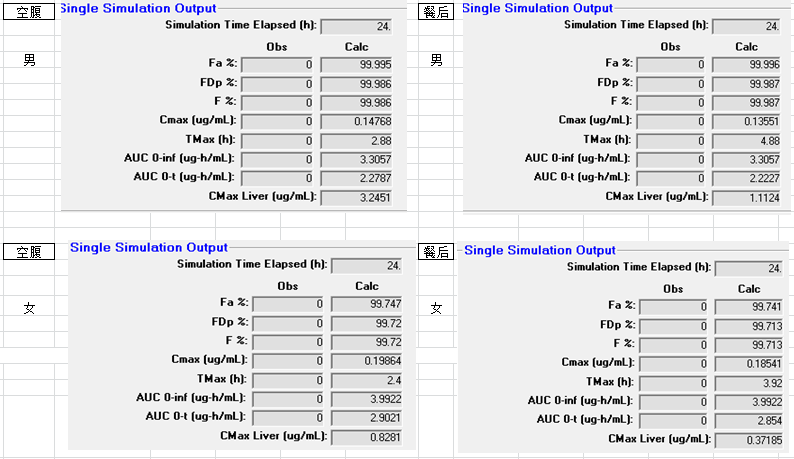
結論:
-
研究結果表明,PK參數受性別影響,處方變更后BCSI類化合物食物對PK參數無顯著影響。建模模擬結果與文獻報道結果相似,運用模型可準確預測處方變更后BCS I類化合物的空腹及餐后PK參數,預測處方變更后食物效應情況。
-
參數敏感性分析表明,在餐后狀態下,化合物1的暴露主要由胃排空時間決定。
甲苯咪唑是一種口服藥物,具有中等親脂性,該化合物具有很強的pH依賴性,在酸性環境(pH 1.0)中溶解度為147μg/mL,在中性環境(pH 7.0)中溶解度為0.67 μg/mL,在堿性環境(pH 12.5)中溶解度為187 μg/mL,在空腹狀態模擬腸液中測定的溶解度為1.08 mg/mL,在餐后狀態模擬腸液中測定的溶解度為3.78 mg/mL,該化合物的滲透率估計很高(Human Peff 10.25*10 ^4cm/s)導致BCS II分類,溶出模型選擇Z-factor模型。
本品理化性質信息如下:
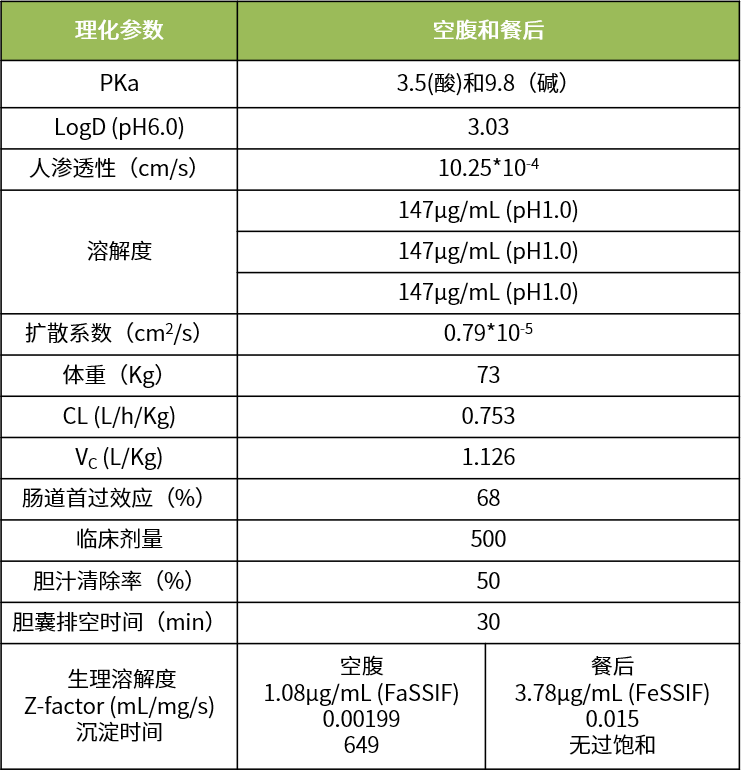
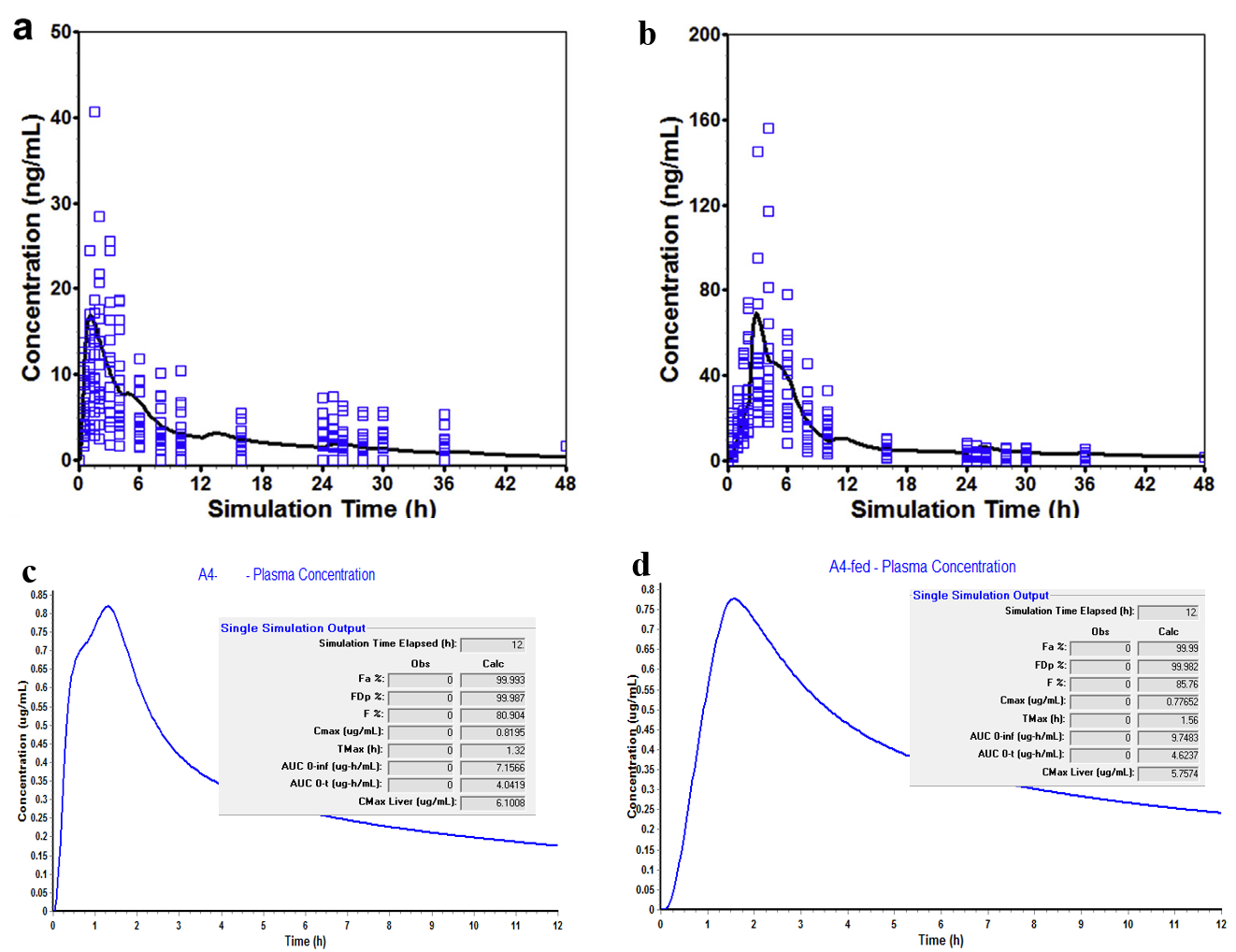
說明:a和b參考文獻中案例2軟件模擬和預測值,c和d是小編建模模擬值,分析由于數據信息欠缺與文獻值有差異,但是小編模擬結果也表明化合物2表現出明顯的正向食物效應。
結論:該BCS II類化合物在服用高脂餐后,膽汁分泌增多具有增溶性,餐后藥物溶解速度和程度普遍提高,導致食物正向效應。
化合物3是一種弱堿,分子量﹤500的親脂性BCS II藥物,其代謝由CYP3A介導,沒有腸道轉運體參與吸收。在生理胃腸道介質中的水溶性在0.1-0.4 mg/mL之間,在Caco-2和PAMPA檢測中具有高滲透性,溶解度具有pH依賴性,在酸性環境(pH 1.0)中溶解度大于5.9 mg/mL,pH 4.6中溶解度0.27 mg/mL,在pH 6.8中溶解度為0.027 mg/mL。IR片劑給藥,在食用一頓低脂餐(Fed LM,~500 kcal)后,評估了人體中化合物3的藥代動力學。單次口服150-300毫克,化合物3表現出快速吸收,中位Tmax為1 ~ 3h(非3h),文獻建模過程中將腸液體積從GastroPlus™的默認值40%和10%改變為 20%和2%,溶出模型選擇Johnson模型。
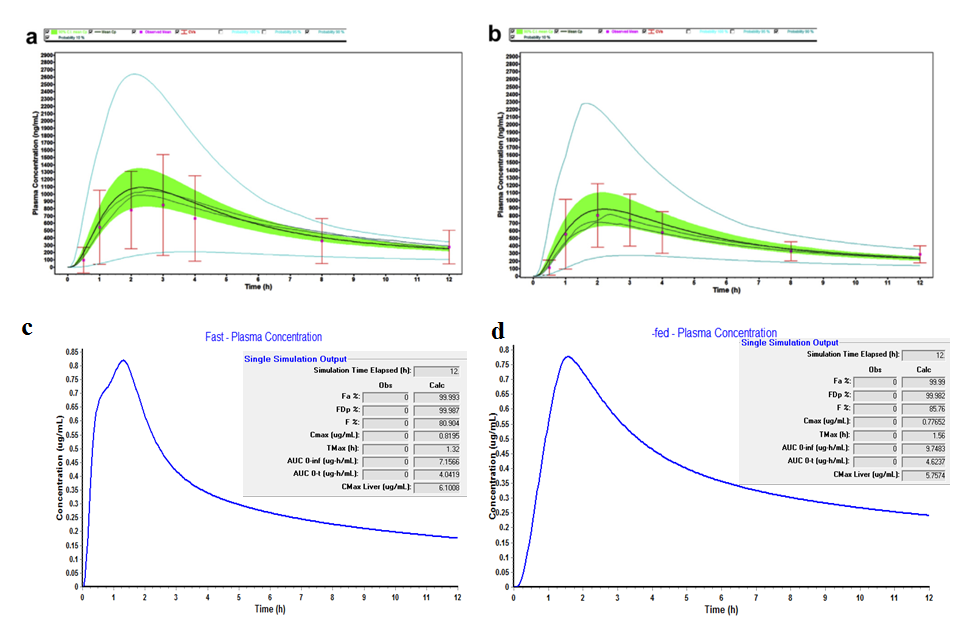
說明:a和b是參考文獻中案例4的軟件模擬和預測值,c和d是小編建模模擬值,小編在模擬過程中發現針對BCSII類弱堿性化合物,溶出模型選擇Johnson模型時,pH對應溶解度對模擬結果影響很大,小編輸入pH1對應溶解度與結果擬合較好,為了與文獻值相似,小編也同文獻將腸液體積從GastroPlus™的默認值進行調整,Cmax模擬結果與文獻相似。
結論:該BCS II類化合物由于預期沒有顯著的食物效應風險,化合物3在臨床試驗中以低脂餐給藥,基于PBPK模型預測結果研究證實化合物3無顯著的食物效應。
基于食物效應可以通過軟件預測模擬預測餐后的BE風險。對于口服藥物,食物可以通過胃腸道生理的各種變化來改變吸收,如胃排空時間、pH值和膽酸鹽濃度等,可能的食物效應主要由兩種機制決定:
-
胃排空時間的影響(對BCS I類化合物最為關鍵)
-
脂質和膽鹽濃度對胃腸道溶解度和溶解速率的影響(對BCS II類化合物最為常見)
值得一提的是,膽汁膠束增溶不一定會導致積極的食物效應,因為化合物在膠束中被包裹,可通過腸細胞膜滲透的藥物的游離部分減少;對于具有高首過效應的BCS II類化合物,考慮攝入食物后內臟血流的變化可能會改善食物效應的預測。
食物效應的PBPK模型可以作為新劑量和處方或原料藥組成的食物效應研究的替代方法,就像體內外相關性(傳統的或基于PBPK)作為相對生物利用度/生物等效性研究的替代方法一樣。在可能難以在健康志愿者中進行臨床研究的情況下化合物(例如腫瘤藥物),這些模型的應用可能更為關鍵。在評估PBPK模型用于臨床開發實用性時,應該考慮對模型預測比率預期范圍內的置信度評估,以及食物效應與暴露關系和特定藥物的安全性。
-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
